
Pada tahun 2010, Kementerian Kesehatan Republik Indonesia mengeluarkan beberapa regulasi penting terkait produksi alat kesehatan dan produk rumah tangga. Regulasi tersebut meliputi PERMENKES 1189/VIII/2010 yang berkaitan dengan produksi alat kesehatan; PERMENKES 1191/VIII/2010 yang mengatur distributor alat kesehatan; dan PERMENKES 70/2010 yang fokus pada produsen rumah tangga. Dengan diperkenalkannya regulasi presiden terbaru, No. 91/2017 dan 24/2018, yang bertujuan untuk percepatan bisnis dan integrasi layanan perizinan secara elektronik, Kementerian Kesehatan telah menerapkan kerangka regulasi baru untuk menyederhanakan layanan perizinan di sektor kesehatan, sehingga mempercepat proses perizinan alat kesehatan di Indonesia.
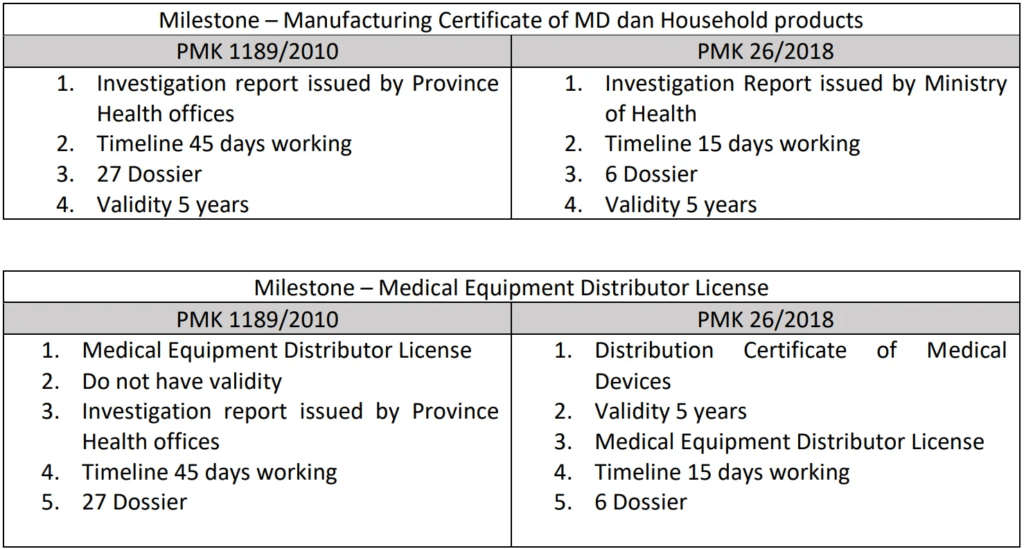
Menurut regulasi sebelumnya, perusahaan yang terlibat dalam produksi dan distribusi alat kesehatan diwajibkan untuk memperoleh lisensi produksi dan lisensi distributor alat kesehatan. Proses ini melibatkan investigasi oleh dinas kesehatan daerah berdasarkan domisili perusahaan. Namun, regulasi baru PMK 26/2018 memindahkan tanggung jawab investigasi kepada pemerintah pusat (Kementerian Kesehatan), sehingga lebih mempercepat proses perizinan. Selain itu, regulasi baru ini juga mengurangi persyaratan, memperpendek timeline, dan menetapkan masa berlaku lisensi distributor selama lima tahun.
Kementerian Kesehatan mengawasi sekitar 33 sektor kesehatan, yang mencakup persetujuan produk untuk alat kesehatan, diagnostik in vitro (IVD), produk rumah tangga, sertifikat distribusi, dan sertifikasi GDPMD (Good Distribution Practice for Medical Devices).
Sejalan dengan regulasi presiden mengenai layanan perizinan elektronik yang terintegrasi, pemerintah Indonesia meluncurkan sistem baru pada Juli 2018 yang disebut OSS (Online Single Submission). Sistem ini mengharuskan semua proses izin dan perizinan, termasuk perizinan alat kesehatan, dilakukan melalui pendekatan satu pintu.
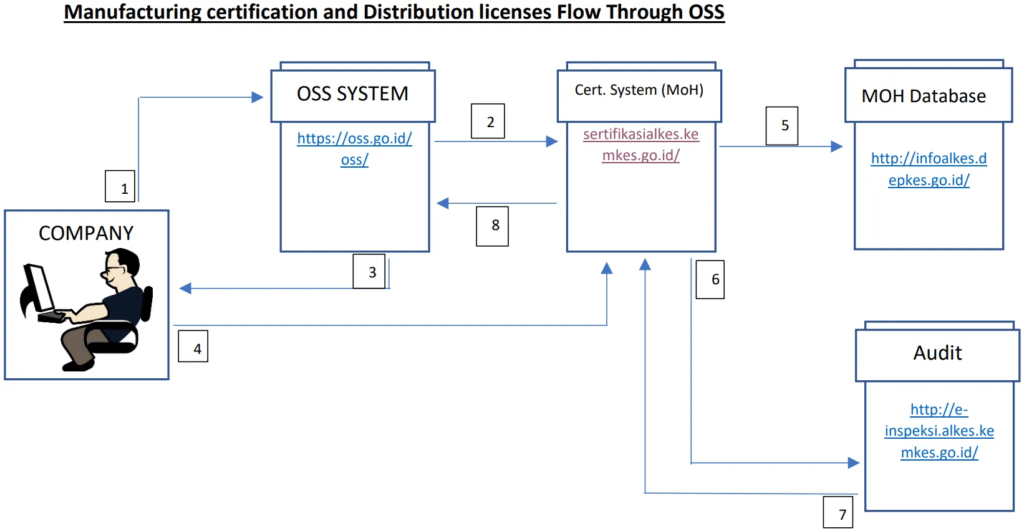
Meskipun masih belum pasti kapan regulasi ini akan sepenuhnya diterapkan di semua sektor kesehatan, perubahan sedang aktif berlangsung. Menurut regulasi 26/2018, Bab IV, tiga kepala pemerintah yang berwenang mengeluarkan izin adalah Kementerian Kesehatan, gubernur daerah, dan bupati atau walikota. Secara khusus, Kementerian Kesehatan bertanggung jawab atas perizinan persetujuan produk, lisensi produksi, lisensi distribusi, dan sertifikasi GDPMD.
Artikel Lainnya
-

Perubahan Kode Klasifikasi Usaha Alat Kesehatan (KBLI): Pemerintah Terbitkan KBLI 2025
-

Pengumuman Penutupan Sistem MoH untuk Pemeliharaan Akhir Tahun
-

Kewajiban Pelaporan Audit Internal Bagi Perusahaan Alkes Pemegang Sertifikat CDAKB
-

Pembaharuan Daftar Laboratorium Pengujian Alat Kesehatan dan PKRT Terakreditasi SNI ISO/IEC 17025:2017
-

Kementerian Kesehatan Indonesia Mengakui Dried Blood Spot sebagai Alat Medis IVD
Layanan Kami
- Perwakilan Lisensi
- Registrasi Produk
- Layanan Pendirian PT Alat Kesehatan
- Perpanjangan dan Perubahan Izin Edar
- Sertifikat Lain- Lain
- Pengawasan Pasca Pemasaran
- E- Katalog
- Pengurusan Merek Alat Kesehatan
- CDAKB (Cara Distribusi Alat Kesehatan Yang Baik)
- Intelejen Regulasi
- IDAK (Izin Distributor Alat Kesehatan)